337. Hãy điền những từ hoặc cụm từ thích hợp: độ tan, dung dịch bão hoà, dung dịch chưa bão hoà, chất tan, nhiệt độ, áp suất
a) …………. là dung dịch có thể hoà tan thêm……………ở nhiệt độ xác định …….. là dung dịch không thể hoà tan thêm ……….ở nhiệt độ xác định.
b) Ở nhiệt độ xác định, số gam chất có thể tan trong 100g nước để tạo thành ……….được gọi là…………. của chất.
c) Yếu tố ảnh hưởng đến độ tan của đa số chất rắn là ………. độ tan của chất khí trong nước sẽ tăng nếu ta giảm ……….. và tăng …………..
338. Bảng dưới đây cho biết độ tan của 3 muối trong nước ở những nhiệt độ khác nhau:
| Nhiệt độ của dung dịch (oC) |
Độ tan (g/100g nước) |
| HgCl2 |
KCL |
Na2SO4 |
| 20 |
7 |
34 |
25 |
| 40 |
10 |
40 |
50 |
| 60 |
15 |
45 |
48 |
| 80 |
25 |
50 |
45 |
| 100 |
0 |
55 |
42 |
a) Qua bảng độ tan của 3 muối trên, em có nhận xét gì về độ tan của chất rắn?
b) Vì sao nhiệt độ chỉ ghi tới 100°C?
339. Hãy chọn câu trả lời đúng nhất.
Độ tan của một chất trong nước ở nhiệt độ xác định là:
A. Số gam chất đó có thể tan trong 100g dung môi để tạo thánh dung dịch bão hoà.
B. Số gam chất đó có thể tan trong 100g dung dịch.
C. Số gam chất đó có thể tan trong 100g nước.
D. Số gam chất đó có thể tan trong 100g nước để tạo thành dung dịch bão hoà.
340. Hãy chọn câu trả lời đúng:
Nồng độ phần trăm của dung dịch là:
A. Số gam chất tan trong 1 lít dung dịch.
B. Số gam chất tan trong 100g dung dịch.
C. Số gam chất tan trong 100g dung môi.
Nồng độ mol của dung dịch là:
D. Số mol chất tan trong 1 lít dung môi.
E. Số mol chất tan trong một thể tích dung dịch xác định.
F. Số mol chất tan trong 1 lít dung dịch.
341. Hoà tan 7,18g muối NaCI vào 20g nước ở 20°C thì được dung dịch bão hoà. Độ tan của NaCL ở nhiệt độ đó là
A. 35g
B. 35,9g
C. 53,85g
D. 71,8g.
Hãy chọn câu trả lời đúng.
342. Độ tan của KCL ở 40°C là 40g. số gam KCL có trong 350g dung dịch bão hoà ở nhiệt độ trên là:
A.150g
B.100g
C.90g
D.50g.
343*. Biết độ tan của muối NH4CL ở 20°C là 37,2g. Hỏi có bao nhiêu gam muối NH4CL trong 300g dung dịch NH4CL bão hoà?
344*. a) Độ tan của muối ăn (NaCI) ở 20°C là 36g. Xác định nồng độ phần trăm của dung dịch bão hoà ở nhiệt độ trên.
b) Dung dịch bão hoà muối NaNO3 ở 10°C là 44,44%. Tính độ tan của NaNO3.
345*. a) Hoà tan 2g NaCI trong 80g H2O. Tính nồng độ phần trăm của dung dịch.
b) Chuyển sang nồng độ phần trăm dung dịch NaOH 2M có khối lượng riêng D = 1,08 g/ml.
c) Cần bao nhiêu gam NaOH để pha chế được 3 lít dung dịch NaOH 10% biết khối lượng riêng của dung dịch là 1,115 g/ml?
346. a) Khi làm bay hơi 50g một dung dịch muối thì thu được 0,5g muối khan. Hỏi lúc đầu, dung dịch có nồng độ bao nhiêu phần trăm?
b) Hoà tan 25g CaCL2.6H2O trong 300ml nước. Dung dịch thu được có D là 1,08 g/ml. Tính nồng độ phần trăm của dung dịch rồi chuyển sang nồng độ mol.
347. Muốn thêm nước vào 2 lít dung dịch NaOH 1M để thu được dung dịch có nồng độ 0,1 M thì lượng nước phải thêm vào là:
A. 20 lít
B. 16 lít
C. 18 lít
D. 22 lít.
Hãy chọn đáp số đúng.
348. Hoà tan 25g chất X vào 100ml H2O, dung dịch có khối lượng riêng là 1,143 g/ml. Nồng độ phần trăm và thể tích dung dịch lần lượt là:
A. 30% và 100ml
B. 25% và 80ml
C. 35% và 90ml
D. 20% và 109,4 ml
Hãy chọn đáp số đúng.
349. Hoà tan 5,72g Na2CO3.10H2O (xôđa tinh thể) vào 44,28ml nước. Nồng độ phần trăm của dung dịch thu được là:
A. 4,24%
B. 5,24%
C. 6,5%
D. 5%.'
Hãy giải thích sự lựa chọn.
350. Người ta pha 40g nước vào 80g dung dịch NaOH có nồng độ 30%. Nồng độ phần trăm của dung dịch NaOH thu được là:
A. 30%
B. 40%
C. 20%
D. 25%.
Hãy chọn đáp số đúng.
351. Hoà tan NaOH vào 200g nước để thu được dung dịch có nồng độ 8%. Khối lượng NaOH cần dùng là:
A. 18g
B. 16g
C. 20g
D. 17,39g.
Hãy chọn đáp số đúng.
352. Khối lượng riêng của dung dịch KOH 12% là 1,1 g/ml. Nồng độ mol của dung dịch KOH 12% là:
A. 2M
B.3M
C. 2,36M
D. 4M.
Hãy giải thích sự lựa chọn.
353*. a) Tính nồng độ mol của dung dịch thu được nếu như người ta cho thêm nước vào 400g dung dịch NaOH 20% để tạo ra 3 lít dung dịch mới.
b) Cho 40ml dung dịch NaOH 1M vào 60ml dung dịch KOH 0,5M. Nồng độ mol của mỗi chất trong dung dịch lần lượt là:
A. 0,2M và 0,3M
B. 0,3M và 0,4M
C. 0,4M và 0,1 M
D. 0,4M và 0,3M.
Hãy giải thích sự lựa chọn.
354. a) Cho thêm nước vào 150 gam dung dịch axit HCL nồng độ 2,65% để tạo 2 lít dung dịch. Tính nồng độ mol của dung dịch thu được.
b) Cho 160ml dung dịch H2SO4 40% có D = 1,31 g/ml. số moỉ H2SO4 có trong dung dịch đó là:
A. 0,8 mol
B. 0,43 mol
C. 0,9 mol
D. 0,86 mol.
Hãy chọn đáp số đúng.
355*. a) Phải lấy bao nhiêu ml dung dịch H2SO4 96%, khối lượng riêng là 1,84 g/ml để trong đó có 2,45g H2SO4?
b) Cho sản phẩm thu được khi oxi hoá hoàn toàn 5,6 lít khí sunturơ (đo ở đktc) vào trong 57,2ml dung dịch H2SO4 60% có D = 1,5 g/ml. Tính nồng độ phần trăm của dung dịch axit thu được.
356*. a) Cần lấy bao nhiêu ml dung dịch có nồng độ 36% (D = 1,19g/ml) để pha 5 lít HCL có nồng độ 0,5M?
b) Cho bột nhôm dư vào 200ml dung dịch HCL 1M ta thu được khí H2 bay ra.
(1) Viết phương trình phản ứng và tính thể tích khí H2 bay ra (điều kiện tiêu chuẩn).
(2) Dẫn toàn bộ khí hiđro bay ra đi qua ống đựng bột CuO dư nung nóng thì thu được 5,76 gam Cu. Tính hiệu suất của phản ứng này.
HƯỚNG DẪN GIẢI, ĐÁP SỐ
337. a) Dung dịch chưa bão hoà là dung dịch có thể hoà tan thêm chất tan ở nhiệt độ xác định. Dung dịch bão hoà là dung dịch không thể hoà tan thêm chất tan ở nhiệt độ xác định.
b) Ở nhiệt độ xác định, số gam chất có thể tan trong l00g nước để tạo thành dung dịch bão hoà được gọi là độ tan của chất.
c) Yếu tố ảnh hưởng đến độ tan của đa số chất rắn là nhiệt độ; độ tan của chất khí trong nước sẽ tăng nếu ta giảm nhiệt độ và tăng áp suất.
338. a) Độ tan của đa số chất rắn thường tăng khi nhiệt độ tăng. Chất rắn Na2SO4 không theo quy luật trên, độ tan giảm khi nhiệt độ càng tăng. Ở 40°C chất tan nhiều nhất là Na2SO4.
b) Ở nhiệt độ trên 100°C, dung môi là nước sẽ bay hơi, khiến cho độ tan của chất không xác định được.
339. Câu trả lời đúng: D.
340. Câu trả lời đúng: B và F.
341. Đáp số đúng: B.
342. Đáp số đúng: B.
343*. Khối lượng NH4CL trong 300g dung dịch NH4CL bão hoà:
m = 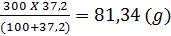 344*. a) l00g nước ở 20°C hoà tan 36g muối ăn
344*. a) l00g nước ở 20°C hoà tan 36g muối ăn
Trong 136g dung dịch chứa 36g muối ăn
Vậy trong l00g dung dịch chứa x g muối ăn
x = 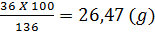
Nồng độ của dung dịch muôi ăn ở 20°C là 26,47%.
b) Trong l00g dung dịch muối NaNO3 có 55,56g nước hoà tan 44,44g NaNO3
x = 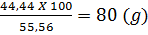
Độ tan của muối NaNO3 ở 10°C là 80 gam.
345*. a) Theo định nghĩa C% tính bằng số gam chất tan có trong l00g dung dịch. Ta có:
C% = 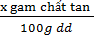 =
= 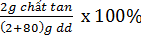
b) Áp dụng công thức: m = V x D
1 lít dung dịch NaOH 2M (D = 1,08 g/ml) có khối lượng 1080g.
Trong 1080g dung dịch NaOH 2M có 80g
Vậy l00g xg
xg
x = 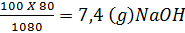
346. a) Trong 50g dung dịch có 0,5g muối khan.
Vậy trong l00g dung dịch có x g muối khan
x = 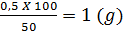
Vậy nồng độ ban đầu là 1%.
b) CaCl2.6H2O = 111 + 108 = 219.
Gọi số gam CaCl2 trong 25g CaCl2.6H2O là x.
Ta có: 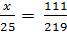 -> x = 12,7 (g)
-> x = 12,7 (g)
Coi khối lượng 300ml nước là 300g (D của nước = 1) thì khối lượng cả dung dịch là:
300g + 25g = 325g
C%(CaCl2) = 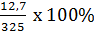 = 3,9%
= 3,9%
- Áp dụng công thức:
CM = C% 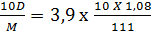 = 0,38 (mol/l)
= 0,38 (mol/l)
CM = 0,38 mol/l hay 0,38M
- Hoặc có thể tính theo cách sau:
Trong 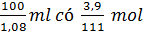 CaCl2.
CaCl2.
Vậy 1000ml có CM = 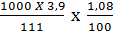 = 0,38 (mol/l)
= 0,38 (mol/l)
347. Đáp số đúng: C
Trong 2 lít dung dịch NaOH 1M có 2 mol NaOH
Trong 1 lít dung dịch sau khi pha loãng có 0,1 mol NaOH
Trong x lít dung dịch sau khi pha loãng có 2 mol NaOH
x = 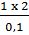 = 20 (lít)
= 20 (lít)
Vậy lượng nước phải thêm 20 - 2 = 18 (lít).
348. Đáp số đúng: D
C% = 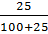 100% = 20%.
100% = 20%.
Thể tích dung dịch: V = 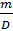 =
= 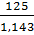 = 109,4 (ml).
= 109,4 (ml).
349. Đáp số đúng: A
350. Đáp số đúng: C
- Tính khối lượng NaOH trong 80g dung dịch 30%.
- Tính khôi lượng dung dịch sau khi pha trộn, lập tỉ lệ
mctmdd x 100%
351. Đáp số đúng: D.
352. 1 lít dung dịch = 1000ml dung dịch; MKOH = 56g
mdd = 1,1 x 1000 = 1100 (g)
Do đó: mKOH = 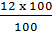 = 132 (g) ; nKOH =
= 132 (g) ; nKOH = 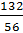 = 2,36 (mol)
= 2,36 (mol)
Nồng độ mol của dung dịch KOH 12% là 2,36M.
353*. a) - Tính khối lượng NaOH trong 400g dung dịch NaOH 20%, từ đó suy ra số mol NaOH.
- Tính CM dựa vào công thức: CM = 
b) Đáp số đúng: D.
354. a) Trong l00g dung dịch khi chưa pha loãng có 2,65g HCl.
Trong 150g  xg HCL
xg HCL
x = 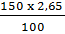 = 3,975 (g) HCL
Số mol HC1 =
= 3,975 (g) HCL
Số mol HC1 = 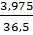 = 0,109 (mol) HCL
= 0,109 (mol) HCL
Trong 2 lít dung dịch có 0,109 mol HCL
Vậy trong 1 lít dung dịch có 0,0545 mol HCL
CM = 0,0545M.
b) Đáp số đúng: D
Áp dụng công thức m = V x D
Khối lượng dung dịch là: 160 x 1,31 = 209,6 (g)
Trong l00g dung dịch có 40g H2SO4
209,6g  xg H2SO4
xg H2SO4
x = 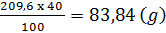 H2SO4
H2SO4
nH2SO4 = 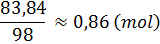 355*. a) Trong l00g dung dịch có 96g H2SO4
355*. a) Trong l00g dung dịch có 96g H2SO4
Trong xg  2,45g H2SO4
2,45g H2SO4
x = 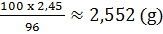 dung dịch
dung dịch
Thể tích dung dịch cần phải lấy = 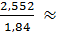 1,387 (ml)
1,387 (ml)
b) nSO2 = 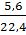 = 0,25 (mol)
= 0,25 (mol)
PTHH
2SO2 + O2 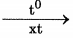 2SO3 2SO3 |
2 mol
0,25 mol |
2 mol
0,25 mol |
mSO3= 0,25 x 80 = 20 (g)
Khối lượng dung dịch axit ban đầu là:
57,2 x 1,5 = 85,8 (g)
Trong 85,8g dung dịch có 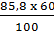 = 51,48 (g) H2SO4
= 51,48 (g) H2SO4
| SO3 + H2O -> H2SO4 |
1 mol
0,25 mol |
1 mol
0,25 mol |
mH2SO4 = 0,25 x 98 = 24,5 (g)
mdd sau phản ứng = 20 + 85,5 = 105,8(g)
C% (H2SO4)= 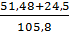 x 100%= 71,8%
x 100%= 71,8%
356*. a) mHCL = 5 x 0,5 x 36,5 = 91,25 (g) HCl
mdd HC1 36% cần dùng là: 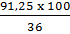 = 253,47 (g)
= 253,47 (g)
Vdd cần dùng: 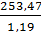 = 213 (ml)
= 213 (ml)
b) (1) nHCl = 0,2 x 1 = 0,2 (mol)
2Al + 6HC1 -> 2A1C13 + 3H2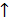 |
2 mol
|
6 mol
0,2 mol → |
3 mol
0,1 mol |
VH2 = 0,1 x 22,4 = 2,24 (lít)
(2) nCu thu được = 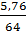 = 0,09 (mol)
= 0,09 (mol)
| H2 + CuO -> H2O + Cu |
| 1 mol |
1 mol |
Nếu hiệu suất phản ứng 100% thì nCu sinh ra bằng nH2 phản ứng và bằng 0,1 mol
H% = 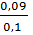 x 100% = 90%.
x 100% = 90%.